实验室制取二氧化碳的化学方程式反应类型是什么?
实验室制取二氧化碳的反应类型是固液常温型反应。实验室中制取二氧化碳,通常采用大理石或石灰石与稀盐酸反应。这是因为大理石和石灰石的主要成分是碳酸钙,当与稀盐酸混合时,会发生化学反应生成二氧化碳。
实验室制取二氧化碳的化学方程式反应类型是分解反应。方程式:CaCO3+2HCl==CaCl2+H2O+CO2↑。注意:(1)制取CO2不能用稀硫酸与大理石(或石灰石)反应,因为反应CaCO3+H2SO4==CaSO4+H2O+CO2↑,生成的CaSO4微溶于水,在溶液中析出后包裹在大理石(或石灰水)的外面,阻碍了反应的进一步发生。
属于复分解反应,实验室制取二氧化碳,一般用石灰石(或大理石)和稀盐酸。化学方程式:CaCO3+2HCl=CaCl2+H2O+CO2↑。
实验室制取二氧化碳,一般用石灰石(或大理石)和稀盐酸,属于复分解反应。化学方程式:CaCO3+2HCl=CaCl2+H2O+CO2↑。反应现象:白色沉淀逐渐消失,同时产生大量气泡,并伴随着大量热的释放,产生的气体能使澄清石灰水变浑浊,由于是稀盐酸,刺激性气味并不明显。
制取二氧化碳的化学方程式是:CaCO3 + 2HCl → CaCl2 + H2O + CO2↑。在实验室中,常用大理石或石灰石(主要成分为碳酸钙)与稀盐酸反应来制取二氧化碳。
实验室制取二氧化碳的三个化学式分别是什么
实验室制取二氧化碳的三个化学式为: CaCO + 2HCl = CaCl + HO + CO NaCO + 2HCl = 2NaCl + HO + CO CaCO 高温分解生成 CaO 和 CO。
碳酸钠与稀硫酸反应:Na2CO3 + H2SO4 → Na2SO4 + CO2↑ + H2O 在实验室制取二氧化碳时,通常会使用上述化学反应。为了确保气体的纯度,可能需要通过饱和的碳酸氢钠溶液除去氯化氢,并通过浓硫酸干燥气体,以去除水蒸气。
在实验室中,有三种常见的方法可以制取二氧化碳。首先,通过碳酸钙(CaCO3)与盐酸(HCl)反应,化学方程式为:CaCO3+2HCI=CaCl2+H2O+CO2。其次,使用碳酸钠(Na2CO3)与盐酸反应,反应式为:Na2CO3+2HCl=2NaCl+H2O+CO2。
实验室制取二氧化碳,一般用石灰石(或大理石)和稀盐酸。化学方程式:CaCO3+2HCl=CaCl2+H2O+CO2↑。
实验室制取二氧化碳注意事项
注意事项:(1)制取二氧化碳时,不能将稀盐酸换成浓盐酸。因为浓盐酸具有挥发性,使制得的二氧化碳混有氯化氢而不纯。制取二氧化碳时,不能将稀盐酸换成稀硫酸。因为碳酸钙与稀硫酸生成的硫酸钙(CaSO) 微溶于水,覆盖在碳酸钙表面,阻止稀硫酸与碳长。
实验室制取二氧化碳通常使用稀盐酸和碳酸钙的反应原理进行操作,实验过程中的注意事项具体如下:实验前检查装置气密性。实验如果用长颈漏斗,应注意末端伸入到液面下液封。使用块状石灰石而不是粉末状石灰石。原因是,防止反应速度过快导致难以收集气体。不用碳酸钠的原因与此相同。
注意事项:- 不要将稀盐酸替换为浓盐酸,因为浓盐酸具有挥发性,会导致制得的二氧化碳中混有氯化氢,从而使气体不纯。- 同样,不要使用浓硫酸代替稀硫酸,因为生成的微溶硫酸钙会覆盖在石灰石表面,阻止进一步的反应。
实验室制取二氧化碳注意事项 制取CO2不能用稀硫酸与大理石(或石灰石)反应,因为会发生反应:CaCO3+H2SO4==CaSO4+H2O+CO2↑,生成的CaSO4微溶于水,在溶液中析出后包裹在大理石(或石灰水)的外面,阻碍了反应的进一步发生。制取CO2一般不选用浓盐酸,因其挥发出HCl气体,使收集到的CO2不纯。
将反应物放入锥形瓶中,通过反应导管将稀盐酸滴加到反应物上,开始反应制取二氧化碳。确保收集装置已准备好以接收气体。 收集与储存 随着二氧化碳气体的生成,通过导管进入收集装置进行收集。将收集好的二氧化碳储存于适当容器中,或进行后续实验。
实验室氮气发生器
因此,根据你们的具体情况,如果你们的实验室每月需要大量氮气,建议选择氮气发生器。当然,如果你们的样品数量较少,且每月购买氮气的费用不是特别高,那么使用氮气罐可能更为方便。
您好,关于氮气发生器的品牌和型号,市场上有很多选择。比如北京中惠普,他们的产品系列包括GCN-1000和SPN-300型号,这些产品在太原衡天力也有销售。北京中惠普是一家专注于气体发生器生产的公司,其产品覆盖了不同需求的用户群体。
您好,进口氮气发生器具有以下特点:智能监控,实时显示氮气纯度,确保产品质量。维护成本低,无需更换或添加分子筛,降低维护费用。特别隔音设计,机器运行时噪音小。无需排水,采用独特技术,省去排水困扰。流量可调节与监控,便于了解实验室仪器使用情况。即插即用,无需连接外部压缩机。
NG-M35氮气发生器的高流量和高压特性,使得远程供气成为可能,尤其适用于需要为多台设备供气的实验室。总体来看,从长期安全和便捷性角度看,替换钢瓶为氮气发生器是实验室改造的理想选择。
东宇在与客户的交流中,发现使用在仪器上的氮气发生器未有实时纯度监测,这引发了对于使用氮气质量的担忧。在意识到实验室因缺乏关注而使用低阶氮气发生器后,客户推荐了东宇跨足实验室领域,以期为客户提供高质量产品,给实验室带来新气象。东宇于2014年开始在区域实验室推广其产品,获得了广泛好评。
在选购氮气发生器时,首要考虑的是厂家的信誉。市面上的设备品牌繁多,质量却良莠不齐。为了确保设备的高质量,推荐选择那些持有特种设备制造许可证的制造商。其中,立可吹氮气发生器是一个值得信赖的选择,我们实验室已经使用了一段时间,效果显著,表现极佳。
实验室制取二氧化碳的方法
1、CaCO3 + 2HCl → CO2↑ + CaCl2 + H2O 这是一种常见的制取二氧化碳的方法,通过观察气泡的产生可以确认二氧化碳的生成。 石灰石与稀硫酸反应:CaCO3 + H2SO4 → CaSO4 + H2O + CO2↑ 由于硫酸钙微溶于水,可能会覆盖在石灰石表面阻止反应,因此这种方法较少使用。
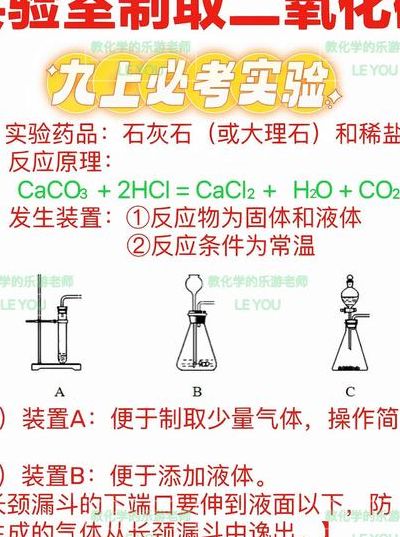
2、实验室制取二氧化碳是用用石灰石和稀盐酸反应而得 反应原理 CaCO3+2HCl=CaCl2+H2O+CO2↑ 仪器装置(如下图所示) 实验步骤 “查”:检查装置的气密性。“装”:从锥形瓶口装大理石,塞紧塞子。“加”:从长颈漏斗(或分液漏斗)加入稀盐酸。“收”:收集气体。
3、实验室制法 在实验室中,通常通过以下化学反应制取二氧化碳:碳酸盐与酸的反应。例如,使用大理石或石灰石与稀盐酸反应,生成氯化钙、水和二氧化碳。这个反应是二氧化碳常见的实验室制法。 工业制法 工业生产中,主要采用高温煅烧石灰石的方法来制取二氧化碳。
4、CaCO+2HCl==CaCl+HO+CO↑ 二氧化碳的实验室制法。药品:稀盐酸和大理石(或石灰石,主要成分是CaCO)。条件:常温。
5、实验室制取二氧化碳的制备方法发酵气回收法:生产乙醇发酵过程中产生的二氧化碳气体,经水洗、除杂、压缩,制得二氧化碳气。副产气体回收法:氨、氢气、合成氨生产过程中往往有脱碳(即脱除气体混合物中二氧化碳)过程,使混合气体中二氧化碳经加压吸收、减压加热解吸可获得高纯度的二氧化碳气。
6、实验室制取二氧化碳的方法主要有两种。首先,可以通过高温煅烧石灰石或白云石来产生二氧化碳气体,然后通过水洗、除杂和压缩等步骤,制得纯净的二氧化碳气体。其次,可以在实验室中使用大理石或石灰石(主要成分为CaCO)与稀盐酸反应来制取二氧化碳。二氧化碳的应用非常广泛。